Dans le cadre de votre traitement, vous pouvez être amené(e) à participer à un essai (ou étude) clinique.
L'essai clinique est une étape essentielle de la recherche de nouveaux traitements, de nouvelles techniques ou de nouvelles stratégies thérapeutiques.
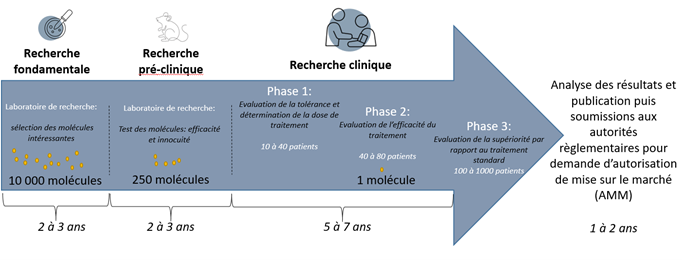
Ces études cliniques sont conformes à la réglementation en vigueur et sont déclarées auprès des autorités compétentes qui donnent leur accord pour leur réalisation en France.
Il existe également des essais cliniques de phase IV qui sont réalisés après la mise sur le marché d'un nouveau médicament pour continuer de recueillir les données de sécurité d'emploi.
Toutes les études se déroulent toujours sous la direction et la surveillance de médecins et d'équipes spécialisés dans ce domaine.